La metformine comme anti-inflammatoire
L’essentiel :
La metformine génère un processus antiinflammatoire
Notamment metformine + fibres solubles + zinc
Le mécanisme d’action serait le suivant : la metformine favoriserait la production par le microbiote intestinal (notamment Akkermansia muciniphila) d’acides gras à très courtes chaînes . En diffusant dans l’abdomen, ceux-ci aurait un effet anti-inflammatoire par exemple sur les intestins, le poumon ? la peau, le cœur, le cerveau ?
La production de ces acides gras particuliers serait potentialisé par les fibres solubles
Une association avec le Zinc serait largement synergique.
/image%2F2354072%2F20201007%2Fob_74f626_metformine.JPG)
La Metformine est un (vieux) médicament utilisé avec succès dans le traitement du diabète sucré (type 2),
Ses effets bénéfiques pourraient être bien plus vastes et inclure des maladies cardiovasculaires, neurodégénératives, certains cancers. Des études (TAME) conduites par la Clinique Mayo sont en cours
Un effet général anti-inflammatoire serait-il à l’origine de toutes ces propriétés ?
« Et si cet effet anti-inflammatoire n’était-il pas, tout simplement, le résultat d’effets sur le microbiote intestinal ? »

Dans une publication de 2010, Thomas Lockwood du Departement de Pharmacologie et Toxicologie de la Wright State University (Dayton, Ohio, USA) propose, résultats à l'appui, ...
d’utiliser la Metformine
(de préférence associée au zinc)
comme agent anti-inflammatoire, dans la thérapie de la polyarthrite rhumatoïde.
en remplacement de la ... chloroquine ! délicate à utiliser.
L'effet anti-inflammatoire de la metformine serait plus général mais pour passer de la metformine et de l’intestin au poumon, voire au coeur, plusieurs étapes sont nécessaires, réunissant des travaux a priori très éloignés.
Prépondérance du microbiote intestinal
Après avoir fait un inventaire de tous les travaux relatifs à l’effet de la metformine dans différents processus métaboliques, comme par exemple : l’inhibition de la chaîne respiratoire des mitochondries, etc.
Benoit Viollet et al., replacent la prépondérance de ces effets dans l’intestin en observant que la metformine s’accumule 30 à 300 fois plus dans les intestins que dans le plasma sanguin.
De son côté, Juan Escobar et ses collègues de l’université de Medellin (Colombie), nous rappelle que « l'intestin est le principal réservoir de la metformine …. [puisque] contrairement à l'administration orale, l'administration intraveineuse de metformine n'améliore pas la glycémie. ».
… confirmant que pour la Metformine, tout se passe dans les intestins, ou presque.
La réponse à ma question : « Et si tous ces effets bénéfiques de la Metformine n’étaient pas, tout simplement, le résultat d’effets sur le microbiote intestinal ? » ... est donc : OUI? ou presque.

Cette hypothèse irait aussi dans le sens des articles du numéro spécial de Pour la science : Intestin. L’organe qui révolutionne la médecine. Notamment :
- La clé de voûte du métabolisme de Rémy Burcelin de l’Université Paul-Sabatier à Toulouse
- Un acteur inattendu de l'immunité de Thomas Pradeu de l’Université de Bordeaux
- Le paradoxe du microbiote de Gérard Eberl, de l’Institut Pasteur de Paris

Plusieurs équipes dont
Yuxin Liu et ses collègues de l’université de Hebei (Baoding, Chine) ont montré que les acides gras à courtes chaînes inhibent :
- la production d’oxyde nitrique (en excès, NO devient un messager pro-inflammatoire)
- ainsi que d’autres pro-inflammatoires, comme les cytokines
La figure ci-contre montre l’effet anti-inflammatoire des acides gras à courtes chaînes (SCFA, cercles bleus) dans les intestins.
Mais, contrairement à ce que laisserait penser ce schéma, les cercles bleus diffusent largement en dehors de l’intestin (voir Axe Intestin-poumon bis)

Plusieurs bactéries du microbiote intestinal produisent ces acides gras très courts, ce sont : Butyrivibrio, Bifidobacterium bifidum, Megasphaera, … et Akkermansia muciniphila : Les "SCFA-producing bacterium" (acides gras à courtes chaînes) sur le schéma ci-contre.
La Metformine est associée à une augmentation de la production de ces acides gras à très courtes chaînes dans les intestins.

Selon Juan Escobar et ses collègues de l’université de Medellin (Colombie), la principale bactérie responsable de cette augmentation de la production d'acides gras à très courtes chaînes (SCFA) est Akkermansia muciniphila.
Akkermansia muciniphila n’est pas une quelconque bactérie présente dans l’intestin, mais faire partie d’une symbiose parfaitement organisée.
Le mucus intestinal est la couche frontière entre l’intérieur et l’extérieur de l’intestin. Les mucus sont constitués de glycoprotéines dont l’architecture constitue un gel.
L’hôte, notamment via les lymphocytes sentinelles de l’intestin …
(leur beaucoup plus large rôle que celui de sentinelle mériterait qu’ils soient dénommés « lymphocytes diplomates »)
… régulent/négocient l’épaisseur du mucus et les propriétés de ses mucines.
La couche de mucus est une source de glucides pour plusieurs bactéries anaérobies intestinales dégradant les mucines dont notamment Akkermansia muciniphila.
Akkermansia muciniphila contribue à réguler la couche de mucus, donc la protection de l’intestin.
Ce rôle s’ajoute celui de fournir des acides gras à très courte chaînes, aux propriétés anti-inflammatoire.
Ce sont les « fibres solubles » de l’alimentation qui permettent au microbiote de fournir le plus de ces Acides gras à très courtes chaînes
« fibre » = longs polymères
« soluble », car les propriétés physico-chimiques de ces fibres leur permettent de former généralement des gels, comme par exemple : les pectines des pommes.
Les « fibres solubles » sont présentes dans de nombreux aliments. Voir : Les fibres alimentaires
De leur côté, Marco Vinolo et ses collègues de l’Institut des Sciences Biomédicales de l’université de Sao Paulo (Brésil) ont publié une revue sur les différents mécanismes anti-inflammatoires des acides gras à très courtes chaînes.
L’un des principaux mécanismes met en jeu une activation d'un des récepteurs aux acides gras à très courtes chaînes : le GPR43 …
Présents à la surface des cellules, les récepteurs aux acides gras à très courtes chaînes sont des « cousins » (par les protéines G) des récepteurs à l’amertume et de ceux au sucré, ce sont :

- GPR41
- GPR43, le plus sensible à l’acétate ;
- GPR109A qui serait plus particulièrement activé par le butyrate, le nicotinate, et des esters de l’acide fumarique
(cette activation par le nicotinate, ou niacine, est sans rapport, sauf historique, avec la nicotine du tabac !)
Le premier bénéficiaire de la diminution de l’inflammation sont les intestins eux-mêmes
La Metformine s’est avérée être capable de réduire l’inflammation du colon (au moins chez la souris)

IBD = inflammatory bowel disease
Voir aussi : La cellulite serait-elle une obésité localisée « là », provoquée par une inflammation « là », qui elle-même provenait d’une inflammation localisée dans l’intestin. Est-ce la même inflammation que celle des diabétiques et/ou des obèses ?
Cellulite. 01. Chouchouter, choyer, bichonner son microbiote

... peut être révélé en deux étapes
1° La conclusion d’Angélica Vieira et son équipe essentiellement de l’Université de Minas Gerais (Belo Horizonte, Brésil) est déterminante :
« le GPR43 [récepteur notamment activé par l’acétate] joue un rôle important dans «l'axe intestin-poumon» en tant que capteur de l'activité du microbiote intestinal de l'hôte … favorisant une réponse immunitaire appropriée [anti-inflammatoire] dans les poumons. »

2° En 2020, François Trottein et ses collègues de l’Institut Pasteur de Lille (France) (auxquels c’étaient joints plusieurs Brésiliens de la Université de Minas Gerais, au Brésil) ont montré :
- d’abord la correspondance entre le changement dans la composition du microbiote intestinal et une surinfection microbienne du poumon.
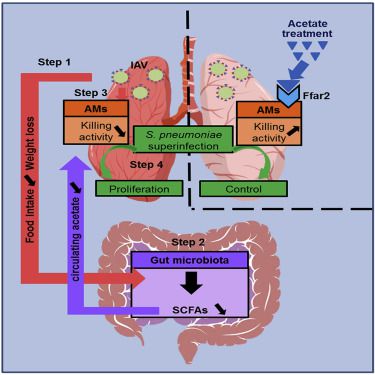
- ensuite qu'un microbiote modifié produisait moins d’acétate et que les poumons étaient davantage susceptibles d’être surinfectées.
A l'inverse, administration d’acétate (un des acides gras à très courtes chaînes) par voie orale permettait de diminuer la propagation bactérienne dans les poumons.
Ces résultats ont été repris dans Pour la Science de mai 2020
Notons que cet effet est rendu physiquement possible par la facilité des acides gras à très courtes chaînes de circuler facilement dans l’organisme.
La solution d’acétate donné à boire aux souris est à 200 mM.
Il s’agit vraisemblablement d’acétate de sodium qui dans le milieu acide de l’estomac doit se transformer en grande partie en acide acétique

Bien entendu, comme moi, cet axe Microbiote intestin– poumon vous a fait penser au Malade imaginaire quand Toinette déguisée en médecin lance :
« Le poumon, le poumon, vous dis-je »
comme origine de tous les maux que décrit Argan.
Nous ne sommes ni les seuls ni les premiers à avoir pensé à Molière !
Marc Humbert, pneumologue à l’hôpital de Bicêtre, l’avait fait avant nous dans un article du Monde de 2015 où il explique le principe du « poumon miroir ».
"Il s’agit d’un miroir à deux faces. D’un côté, certaines maladies pulmonaires se reflètent hors du poumon, par des atteintes de la peau, des doigts, du cerveau, du cœur… A l’inverse, des affections non pulmonaires se présentent parfois comme des maladies du poumon ».
et ajoute :
« Certaines céphalées résultent d’une complication de l’insuffisance respiratoire, qui augmente la pression en dioxyde de carbone dans le sang. »
Le poumon ne serait-il qu'une étape ? un point de passage des acides gras à très courtes chaînes ?
Le point de départ serait-il l’intestin ou plus exactement son microbiote ?
Ces atteintes de la peau, des doigts, du cerveau, du cœur… ainsi que certaines céphalées
… seraient-elles des manifestations d’une perturbation du microbiote intestinal ?

Cette « administration d’acétate par voie orale permettant diminuer la propagation bactérienne dans les poumons. » ne pourrait-elle pas se faire aussi par inhalation ?
Selon la légende, les Quatre voleurs auraient respiré un vinaigre aromatique pour piller les maisons pendant les épidémies de peste, sans être contaminés.
Le principe de cette protection aurait été reprise ensuite par les ... médecins.

Le vinaigre est une solution d’acide acétique, 6% pour un « vinaigre de vin ». L’acétate, quand à lui, est une forme non acide.
Celui utilisé par François Trottein doit être de l’acétate de sodium.
(ci-contre formule d’une ancienne édition de L'Officine ou Répertoire général de la pharmacie pratique, le « Dorvault »)
Le principe actif du Vinaigre des 4 voleurs était-il d’abord l’acétate ?
Parmi des ingrédients, on notera aussi la présence de camphre et d’absinthes
Thomas Lockwood observe, de plus, une spectaculaire (« astounding ») synergie avec l’ion zinc Zn2 + ; qu'il évalue d’un facteur de 10 à 100.
Concernant Zn2 +
- Son utilisation a été évoquée dans plusieurs thérapies visant le coronavirus.
- Un déficit physiologique de zinc peut provoquer une perte de goût (hypogeusie). « Le zinc est un oligo-élément qui intervient dans de nombreuses réactions enzymatiques et joue un rôle important dans le métabolisme … y compris dans comme anti-inflammatoire ...(Doctissimo)

- L’ion Zn2 + a été reconnu par plusieurs équipes comme un activateur d’un récepteur à l’amertume le TAS2R7 dont en 2019 par Peihua Jiang et son équipe internationale
- l’ion zinc stabilise le plissement de plusieurs protéines, la forme particulière de cet agencement a été appelée « doigt de zinc ». Or ce « doigt » est évoqué dans la publication de David Gordon et al. sur le Covid-19
- Comme anti-inflammatoire, le zinc, provoque la baisse des cytokines, par exemple IL-1β ; voir l'article d' Ananda Prasad, de la Wayne State University School of Medicine (Detroit, USA),
Le zinc Zn2+ est un co-facteur du catabolisme des « fibres solubles". Faut-il y voir l’effet amplificateur de l’action de la metformine ?
/image%2F2354072%2F20201007%2Fob_155a84_medscape.JPG)
L’observation selon laquelle « Un taux de zinc plasmatique plus faible est associé à un risque accru de décès chez les patients atteints du COVID-19 » (rapportée par Priscilla Lynch dans Medscape du 6 octobre 2020)
… peut-elle s’expliquer par un effet anti-inflammatoire des Acides gras à très courtes chaînes produits par le microbiote intestinal ?
Concernant la protection de la metformine contre la Covid, voir : Metformine, Covid, Mortalité.

/image%2F2354072%2F20201007%2Fob_b87968_acetate.JPG)